阿伏加德罗常数的考查,几乎可以将中学化学计算兼容到一个题中,所以几乎是高考必考题。考题主要是两种类型:选择题和利用物质的量的简单计算(涉及到大题中的小计算),在高考中所占的分值较大, 阿伏伽德罗常数(NA)是历年高考的热点,经久不衰,常常在考题中有意设置一些极易疏忽的干扰因素。在分析解答这类问题时,要特别注意以下几点:

01、标准状况条件
(1)考查气体时经常给非标准状况如常温常压下,101kPa、25℃时等。
(2)若给出的是气体的物质的量或质量,则求微粒数与外界条件无关。
例如:
11.2L N2 含有 N2分子数为0.5NA(x)
标况下22.4 L以任意比例混合甲烷和丙烷的混合物分子数为NA(√)
常温下32g SO2 气体中含有0.5NA个 SO2 (√)
02、物质状态
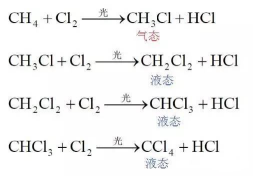
考查气体摩尔体积时,常用在标准状况下非气态的物质来迷惑考生,如H2O、SO3、HF,己烷(C6H14),辛烷(C8H18),二氯甲烷(CH2Cl2),三氯甲烷(CHCl3),四氯化碳(CCl4),HCHO,苯为液态或固态等。
03、微粒问题
考查一定物质的量的物质中含有多少微粒(分子、原子、电子、质子、中子等)时常涉及稀有气体He、Ne、Ar等为单原子分子,Cl2、N2、O2、H2、NO为双原子分子,O3为三原子分子,白磷(P4)、NH3为四原子分子等。
★所求微粒个数与微粒种类必须一一对应★
★要注意特殊物质摩尔质量:
1H:1;2D:2 ;3T:3;
H2O:18g/mol;
D2O:20g/mol;
T2O:22g/mol;
18O2:36g/mol;
Na37Cl :60。★
例如:
1mol氦气含氦原子数为2NA(x)
常温下48g O3 含氧原子数为3NA(√)
10g重水里含有的电子数为5NA(√)
1.8g重水中含有NA个中子(x)
04、晶体结构/化学键数目
常考:SiO2、Si、CH4、P4、CO2、石墨烯、石墨、金刚石
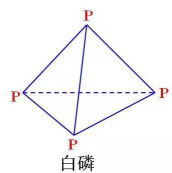
(1)P4(白磷):1mol白磷含4mol磷原子、6molP-P键
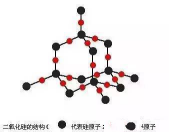
(2)SiO2 晶体:1mol硅原子形成4molSi-O键,需要2molO与之成键
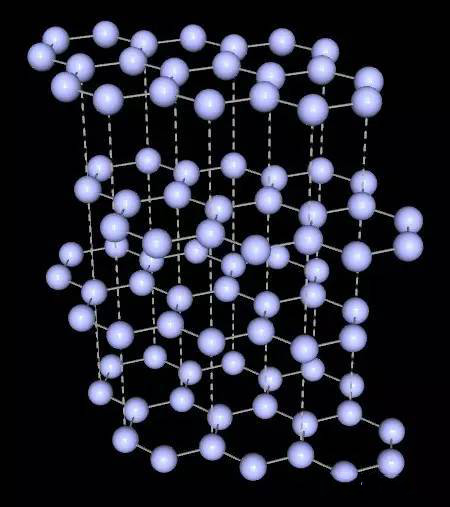
(3)金刚石: 1mol碳形成2molC-C键
【金刚石的晶体结构是一种空间网状结构,每一个碳原子与周围的四个碳原子形成一个正四面体,所以正四面体中心的一个碳原子形成4个C-C单键,该碳原子对一个C-C单键的形成的付出是1/2,所以,正四面体中心的这个碳原子参与形成的C-C单键数目相当于4&x1/2=2,故金刚石中,1mol金刚石可以形成2molC-C单键。】
(4)石墨:1mol碳形成3molC-C键
例如:
31g白磷含0.25NA白磷分子1.5NA个P-P键 (√)
SiO2 晶体中1mol硅原子与2NA个氧原子形成共价键 (√)
05、氧化还原反应
考查指定物质参加氧化—还原反应时,常设置氧化—还原反应中氧化剂、还原剂、氧化产物、还原产物、被氧化、被还原、电子转移(得失)数目方面的陷阱。
如Fe与氯气反应,Fe、Cu与硫反应,氯气与NaOH或H2O反应,Na2O2与CO2或H2O反应等。
2Fe+3Cl2=(点燃)2FeCl3
2Al+3Cl2=(点燃)2AlCl3
【1molFe或Al与足量Cl2反应金属失3NA个电子】
Fe + S=(△)FeS
Cu + S=(△)Cu2S
【64g Cu与足量S反应铜失1NA个电子】
Cl2+ 2NaOH=NaCl+ NaClO+ H2O
Cl2+ H2O ? HCl+ HClO
【1molCl2与NaOH或与H2O反应转移电子数为NA】
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2
【1mol Na2O2与CO2或与H2O反应转移电子数为NA】
06、电离、水解
考查电解质溶液中微粒数目或浓度时常涉及弱电解质的电离,盐类水解方面的陷阱。
07、特例
NO2存在着与N2O4的平衡。
例如:
2NO2?N2O4则标况下4.6g NO2小于2.24L
高考真题
1、【2016年高考新课标Ⅰ卷】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.14 g乙烯和丙烯混合气体中的氢原子数为2NA
B.1 molN2与4 mol H2反应生成的NH3分子数为2NA
C.1 molFe溶于过量硝酸,电子转移数为2NA
D.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
【答案】A
【解析】乙烯和丙烯的最简式都是CH2,14 g乙烯和丙烯混合气体中含有的最简式的物质的量是n(CH2)=m÷M=14 g÷14 g/mol=1 mol,所以其中含有的氢原子数为N(H)=1 molx2xNA=2NA,A正确;N2与H2在一定条件下发生反应生成NH3,该反应是可逆反应,反应物不能完全转化为生成物,故1 mol N2与4 mol H2反应生成的NH3分子数小于2NA,B错误;铁是变价金属,硝酸具有强的氧化性,所以 1 mol Fe溶于过量硝酸生成硝酸铁,反应中电子转移数目为3NA,C错误;在标准状况下四氯化碳是液态,不能用气体摩尔体积进行有关物质的量的计算,D错误。
2、【2016年高考四川卷】 NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.2.4g镁在足量的氧气中燃烧,转移的电子数为0.1NA
B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA
C.氢原子数为0.4NA的甲醇分子中含有的σ键数为0.4NA
D.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
【答案】B
【解析】2.4 g镁的物质的量为2.4/24=0.1 mol,反应中失去0.2 mol电子,A错误;标准状况下5.6 L二氧化碳的物质的量为5.6/22.4=0.25 mol,含有的氧原子为0.5 mol,B正确;甲醇的结构为CH3OH,氢原子数为0.4NA的甲醇分子为0.1 mol,含有5molσ键,C错误;醋酸是弱酸,不能完全电离,D错误。
3、【2016年高考江苏卷】下列说法正确的是()
A.氢氧燃料电池工作时,H2在负极上失去电子
B.0.1mol/LNa2CO3溶液加热后,溶液的pH减小
C.常温常压下,22.4L Cl2中含有的分子数为6.02x1023个
D.室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力增强
【答案】A
【解析】氢氧燃料电池工作时,H2发生氧化反应,在负极上失去电子,A正确;升高温度,促进碳酸钠的水解,溶液的pH增大,B错误;常温常压下,气体的摩尔体积大于22.4L/mol,22.4LCl2中的物质的量小于1mol,含有的分子数小于6.02x1023个,C错误;室温下,稀释稀醋酸,虽然电离平衡正向移动,自由移动离子的数目增加,但溶液体积的增大起主导作用,自由移动离子的浓度减小,溶液的导电能力减弱,D错误。





